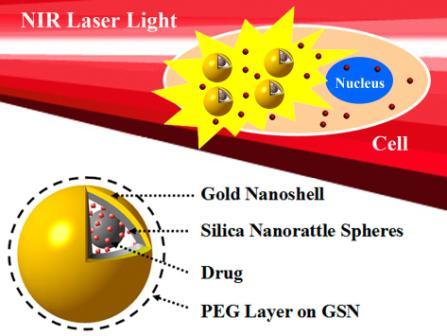
多功能纳米金壳热化疗协同杀死癌细胞示意图
继国际著名学术期刊ACS nano(2010, 4, 6874-6882)和Biomaterials(2011, 32, 1657-1668)相继报道了理化所研制的新型纳米载药系统在恶性肿瘤治疗及其生物安全性评价方面的工作之后,最新一期国际材料界顶级刊物《德国应用化学》 Angewandte Chemie International Edition(2011, 50, 891 –895)报道了理化所在之前工作基础上开展的新型多功能纳米金壳光热化疗结合应用于癌症治疗的新进展。
恶性肿瘤已超过心血管疾病,成为城市居民首要致死病因,严重威胁人类的生命与健康,给社会、家庭和个人带来极大的负担和痛苦。人们期待能够发展一种最小创伤、低剂量、短时间内杀死肿瘤细胞而不伤害正常组织的新型材料。国际最新研究成果表明,利用金壳介电复合结构纳米材料的等离子体共振性质将光能转化为热能治疗恶性肿瘤具备明显的优势和可行性。
唐芳琼研究员带领的纳米材料可控制备与应用研究室创新研制出高产量,可精确控制颗粒尺寸、外壳厚度、内部空腔大小,具有中空和介孔结构的“夹心二氧化硅”(Adv. Mater. 2009, 21, 3804-3807) 后,在纳米夹心二氧化硅制备基础上,创新研制了多功能纳米金壳微创癌症诊治新技术平台。该多功能纳米金壳内层为结构独特的中空介孔夹心二氧化硅,其表面包覆金壳,纳米金壳以其物理化学性质——等离子体共振性质为基础,将光能转化为热能,并配以夹心二氧化硅对多种化疗药物的装载控制缓释技术,既可克服传统热疗技术的非靶向难题,避免热疗过程中对正常组织的损害,同时因其高吸光截面积,高光热转化率,与传统的磁热疗技术相比具有用量少、升温快、创伤小、治疗时间短的优势,同时其热疗与化疗技术的结合与单一金壳光热治疗技术相比更体现综合治疗理念。实验证明,该新型多功能纳米金壳采用光热疗法与化疗药物的缓控释结合,对肝癌的抑瘤率高达85%,单纯游离药物泰素帝抑瘤率仅为57%,且毒副作用很大,动物实验证明该材料可显著降低化疗药物毒副作用。相关工作已申请国际PCT专利。
该工作在线发表后受到相关国际媒体的关注,其中ChemPubSoc Europe (欧洲化学出版协会)旗下的“ChemistryViews”以More Efficient Cancer Treatment为题对该工作进行了介绍。美国纳米材料与纳米技术网“Nanowerk”于2011年1月17日以“Nanowerk Spotlight”形式对该工作进行了专题报道,题为“A step towards highly efficient, minimally invasive and low systemic toxicity cancer therapy”。报道称该团队研究的多功能金壳包覆夹心二氧化硅如同“魔力子弹”,能够将光热治疗与化疗结合协同治疗癌症,与单一金壳光热疗技术或单纯化疗相比更加高效、低毒。
该研究得到国家科技部“863”项目和国家自然科学基金的大力支持。
文章链接:http://onlinelibrary.wiley.com/doi/10.1002/anie.201002820/pdf
ChemistryViews网站点评链接:
http://www.chemistryviews.org/details/ezine/883317/More_Efficient_Cancer_Treatment.html
Nanowerk网站点评链接:
新闻中心